FARMACI
Gli antibiotici vanno utilizzati quando servono e devono essere prescritti dal medico.
Trattamento di supporto delle infezioni delle prime vie respiratorie nel bambino
Generalità
Le infezioni delle prime vie respiratorie sono prevalentemente ad eziologia virale ed includono il raffreddore comune, l'influenza, la laringite, la faringite, la sinusite, la tonsillite ed il croup. Le infezioni delle prime vie aeree rappresentano la causa più frequente di consultazione del pediatra e colpiscono soprattutto i bambini di età inferiore a 2 anni e quelli che frequentano le comunità infantili. Si stima che in media un bimbo nei primi anni di vita abbia più di 4 episodi di infezione delle prime vie aeree1.
Esiste una chiara stagionalità nella circolazione dei virus che sono più frequentemente responsabili di infezioni delle prime vie aeree; in particolare durante l'inverno il virus respiratorio sinciziale, i virus influenzali e i parainfluenzali, gli adenovirus, rinovirus e coronavirus sono i più frequenti agenti eziologici. Più raramente queste infezioni sono sostenute da batteri come lo Streptococcus pneumoniae. Le manifestazioni cliniche di queste infezioni includono sistematicamente congestione e secrezione nasale, starnuti, mal di gola, tosse, malessere generale e febbre. La trasmissione di queste infezioni avviene per via respiratoria attraverso le goccioline di saliva oppure per la contaminazione di superfici e conseguente contatto con le mani. Occasionalmente queste infezioni possono essere seguite da complicazioni batteriche come l'otite media, la sinusite e la polmonite. Talvolta le infezioni delle prime vie aeree possono essere seguite da complicanze anch'esse virali come la bronchiolite, la polmonite o il croup. Le infezioni respiratorie sostenute da virus sono autolimitanti e, sebbene le complicazioni siano un'evenienza rara, data l'elevata frequenza, il loro impatto è notevole sulle prescrizioni farmaceutiche e sul consumo di farmaci da banco. Nonostante queste infezioni procurino sintomi solo per alcuni giorni, e difficilmente oltre una settimana, la presenza dei tipici fastidiosi segni clinici è causa di sistematiche richieste e consumo di farmaci per il loro trattamento.
La gestione delle infezioni respiratorie delle prime vie aeree dovrebbe comprendere i seguenti punti3:
Alcuni preparati associano parte dei farmaci disponibili per il trattamento dei sintomi delle infezioni delle prime vie aeree con altri farmaci che rendono potenzialmente maggiore il rischio di effetti collaterali. Inoltre, paradossalmente, le prove a favore dell'efficacia di questi trattamenti per la risoluzione dei sintomi nelle affezioni respiratorie sono scarse e, per alcuni di essi, sono semplicemente estrapolate da studi effettuati nella popolazione adulta. Queste osservazioni dovrebbero essere sempre considerate nel processo decisionale per la gestione terapeutica. Antipiretici e antinfiammatori
I farmaci da banco come paracetamolo, ibuprofene ed acido acetilsalicilico (ASA) sono i farmaci più utilizzati nel trattamento sintomatico delle infezioni delle prime vie respiratorie. Nonostante il diffuso utilizzo, c'è poca letteratura per questo specifico uso, sia negli adulti che nei bambini. I dati sono quindi estrapolati da studi sulla febbre o sul dolore. Gli autori di una recente revisione sistematica6 hanno analizzato la letteratura per puntualizzare i dati disponibili in termini di efficacia e di sicurezza.
Il paracetamolo è largamente utilizzato per l'effetto antipiretico e antidolorifico. Le dosi raccomandate sono illustrate nella tabella I.
Per quanto riguarda la sicurezza, in una revisione su 40 anni d'uso del paracetamolo nei bambini7, gli autori concludono che "questa molecola rimane la prima scelta tra i farmaci da banco per l'analgesia e l'antipiresi e che quando utilizzata nelle dosi raccomandate ha pochi effetti collaterali essendo sostanzialmente ben tollerata".
Gli effetti collaterali (epato e nefro tossicità) sono dovuti al sovradosaggio. La dose epatotossica è di 150 mg/kg o 75mg/kg nei bambini con rischio aumentato di sviluppare danno epatico (patologie epatiche, malnutrizione, terapia con induttori enzimatici - carbamazepina, fenobarbital, fenitoina, rifampicina - infezione da HIV, patologie metaboliche).
Sull'efficacia dell'ibuprofene, da qualche anno largamente utilizzato come antipiretico in pediatria, sono disponibili prevalentemente studi clinici comparativi con il paracetamolo piuttosto che contro placebo. Molti di questi studi hanno mostrato una equivalenza di efficacia tra le due molecole, soprattutto come azione antipiretica8,9.
In uno studio clinico randomizzato in doppio cieco condotto su bambini con età compresa tra 2 e 12 anni, una singola dose (10 mg/kg) di ibuprofene si è dimostrata efficace e superiore al placebo sia per il trattamento della faringodinia che della febbre associata ad infezione delle prime vie respiratorie10. Anche per l'ibuprofene i dati sulla sicurezza sono rassicuranti. Due revisioni sistematiche analizzano l'efficacia ma anche la sicurezza del paracetamolo e dell'ibuprofene, con dati positivi per entrambe. Un ampio trial clinico randomizzato condotto su 27.065 bambini febbrili con età inferiore a 2 anni ha studiato la sicurezza di: paracetamolo 12 mg/kg, ibuprofene 5 mg/kg e ibuprofene 10 mg/kg. Gli autori concludono che con questi farmaci il rischio di seri effetti collaterali è basso11,12.
Poiché l'ibuprofene appartiene alla categoria dei farmaci antinfiammatori non steroidei (FANS), non va somministrato nei pazienti con ulcera peptica attiva o con anamnesi positiva o con reazioni di ipersensibilità ai FANS. Tuttavia tra gli antinfiammatori viene considerato il più sicuro in termini di effetti gastrointestinali. La letteratura non indica alcun rischio di danno intestinale o sanguinamento per l'uso di breve durata alle dosi utilizzate come antipiretico13-15.
Sebbene vi siano dei vecchi studi sull'efficacia dell'ASA nei bambini, per il rischio di sindrome di Reye l'ASA è controindicato nei bambini con età inferiore ai 12 anni. La sindrome di Reye è una patologia rara ma a rischio di morte ed è tipicamente associata all'uso di ASA in caso di infezioni virali, soprattutto influenza e varicella16-19. Decongestionanti nasali
La congestione nasale è il sintomo che più frequentemente viene riferito in corso di infezioni delle alte vie aeree. I decongestionanti nasali sono rappresentati da una vasta gamma di principi attivi disponibili singolarmente o in associazione, sia sotto forma di preparazioni per uso topico sia sistemico. Si tratta principalmente di due categorie di sostanze: derivati delle catecolamine (amine simpaticomimetiche quali efedrina, fenilefrina, fenilpropanolamina, tuaminoeptano, p-ossifenilpropilamina iodidrato) e derivati imidazolinici (benzilimidazoline come ossimetazolina, xilometazolina; naftimidazoline come nafazolina, tetrizolina, tramazolina, clonazolina). Questi farmaci hanno varie indicazioni autorizzate (per esempio rinite, faringite acuta e catarrale, otite catarrale, processi infiammatori nasali e paranasali, rinite allergica, sinusite acuta, ecc.), ma sono prescritti, o più spesso autosomministrati, per alleviare i sintomi del raffreddore tra cui l'ostruzione nasale. Il meccanismo di azione è mediato dalla vasocostrizione arteriolare indotta da queste sostanze, mentre non vi è influenza sugli altri meccanismi (edema mucosale, essudazione e secrezione fluida nelle vie aeree) che causano i sintomi.
Una revisione sistematica del 2007 analizza 7 studi sull'adulto riguardanti l'utilizzo di decongestionanti nasali in corso di infezione delle alte vie aeree. Confrontati con placebo, i decongestionanti nasali mostrerebbero un piccolo ma statisticamente significativo miglioramento nel ridurre il sintomo (circa il 6%)20. Non sembrerebbe esserci differenza per quanto concerne l'efficacia nell'utilizzo topico o per via orale.
Negli studi identificati dalla revisione non sono stati indagati o riportati effetti avversi; solo due studi infatti hanno riportato i dati di sicurezza, mostrando un'incidenza di reazioni avverse ai decongestionanti relativamente esigua e un piccolo aumento (5%) del rischio di insonnia, per lo più in concomitanza con l'assunzione di pseudoefedrina20.
Da altri studi è noto comunque che i decongestionanti nasali, soprattutto se usati per periodi superiori a 5 giorni, possono indurre reazioni avverse a livello locale, generalmente irritazione locale transitoria; la vasocostrizione indotta dai decongestionanti topici può però essere seguita da vasodilatazione o congestione rebound, che sembra essere meno marcata per i derivati imidazolinici e per l'ossifenil-propilamina iodioidrato. Il paziente, se non avvertito, pensando di sopperire alla ridotta efficacia tende ad incrementare la dose e la frequenza delle somministrazioni per ottenere sollievo dalla congestione secondaria, ignorando che quest'ultima è indotta dallo stesso farmaco.
Nel tempo la ridotta sensibilità dei recettori alfa adrenergici può causare tachifilassi. Per questo motivo il trattamento non deve durare più di 2-5 giorni. L'abuso dei vasocostrittori, indotto dal fenomeno della congestione rebound e della tachifilassi, e lo scorretto uso del farmaco possono determinare alterazioni prolungate della mucosa che risultano in rinite atrofica medicamentosa. Poiché la mucosa nasale è una buona superficie di assorbimento, in circostanze rare quantità significative di questi farmaci possono essere assorbite e causare a livello sistemico effetti simpaticomimetici. Le reazioni avverse più significative sono a carico dell'apparato cardiovascolare (ipertensione arteriosa, tachicardia, pallore, sudorazione, bradicardia, ipotensione arteriosa) e del sistema nervoso centrale - SNC (cefalea, depressione neurologica con sintomi che vanno dalla sonnolenza fino al coma e depressione respiratoria).
Nonostante l'elevata incidenza di raffreddore nei bambini, non sono stati identificati trial sui decongestionanti nasali utilizzati al di sotto dei 12 anni di età che rispondevano ai criteri di inclusione della revisione.
Due trial randomizzati in doppio cieco con placebo che includevano l'utilizzo di antistaminici e decongestionanti in combinazione in bambini da 6 mesi a 5 anni non hanno identificato differenze significative nella durata e nella gravità dei sintomi21,22.
Le differenze esistenti tra la popolazione adulta e quella pediatrica, sia nell'anatomia nasale sia nella tolleranza ai farmaci, non permettono un'estrapolazione dell'efficacia e della sicurezza dei decongestionanti nei bambini.
Nella Rete Nazionale di Farmacovigilanza sono inoltre presenti alcune segnalazioni di reazioni avverse associate a farmaci simpaticomimetici per uso topico, analogamente a quanto avviene a livello internazionale23-25. Riguardano soprattutto bambini molto piccoli (al di sotto di 1 anno e tra 1 e 3 anni), sono gravi e prevalentemente a carico della cute e del tessuto sottocutaneo (reazioni da ipersensibilità, prurito, eritema, edema faringeo, orticaria, sudorazione, necrolisi epidermica, esantema eritematoso), del SNC (ipotonia, torpore, contrazioni muscolari involontarie, pallore, agitazione, sonnolenza, ipercinesia, irritabilità, depressione, letargia), della mucosa nasale (rinite medicamentosa), dell'apparato cardiovascolare (extrasistoli, vasodilatazione, tachicardia, bradicardia), dell'apparato respiratorio (depressione respiratoria, dispnea, apnea, broncospasmo).
A tal proposito nel 2000 la European Accademy of Allergology and Clinical Immunology ha pubblicato il "Consensus statement on treatment of allergic rhinitis" in cui non si raccomanda l'uso di decongestionanti nasali nei bambini molto piccoli a causa dei possibili effetti collaterali e dello stretto range tra la dose terapeutica e quella tossica26.
La maggior parte delle specialità in commercio non è stata testata su pazienti pediatrici, quindi questi prodotti vengono utilizzati off-label ricorrendo, per i dosaggi, all'estrapolazione di dosaggi calcolati per adulti. I bambini quindi rappresentano una popolazione ad alto rischio per le possibili complicanze da sovradosaggio.
I Centers for Disease Control and Prevention (CDC) della Food and Drug Administration hanno indagato sul decesso di tre bambini di età compresa tra 1 e 6 mesi, la cui morte è stata imputata alle altissime concentrazioni di pseudoefedrina plasmatica, e dall'analisi effettuata è emerso che, durante il 2004 e 2005, più di 1500 bambini sono stati ricoverati negli ospedali americani per gli effetti avversi legati ai farmaci per tosse e raffreddore, sovradosaggio compreso. Questi prodotti possono comunque essere acquistati senza ricetta sia in USA che in Europa.
La rivalutazione del profilo beneficio/rischio di questi farmaci nei bambini ha dato esito sfavorevole, pertanto l'Agenzia Italiana del Farmaco ha adottato un provvedimento restrittivo vietando l'uso dei decongestionanti nasali ad attività simpaticomimetica nei bambini al di sotto di 12 anni27. Farmaci per via inalatoria: la terapia aerosolica
Respirare vapore o aria calda è generalmente considerato un aiuto privo di effetti collaterali per trattare la congestione nasale e sinusale. Il beneficio fisico è verosimilmente legato alla liquefazione delle secrezioni respiratorie che permette una rimozione più efficace mediante la tosse o soffiandosi il naso; inoltre si apprezza un effetto lenitivo sulle mucose.
Esistono alcuni studi che hanno tentato di valutare l'effetto dell'inalazione con vapore nel raffreddore comune, tutti condotti su pazienti adulti, che hanno dato risultati contrastanti28-30.
Tenuto anche conto della difficoltà ad eseguire una terapia aerosolica ad un bambino e vista la scarsità delle evidenze per sostenere tale indicazione, non è da considerarsi un trattamento risolutivo. L'utilizzo di ribavirina o antibiotici per via aerosolica è segnalato in categorie di pazienti a rischio e pertanto non è da considerarsi una pratica routinaria31,32. Non esistono studi che valutino l'efficacia e la tollerabilità di steroidi per via inalatoria negli episodi respiratori acuti delle vie aeree superiori che non siano associati ad asma o wheezing. Sedativi della tosse
L'uso dei sedativi della tosse nelle affezioni delle prime vie aeree in età pediatrica è controverso e largamente basato sull'estrapolazione di studi clinici effettuati negli adulti. La tosse è un meccanismo fisiologico di protezione che ha lo scopo di eliminare le secrezioni dell'albero respiratorio e di mantenere pervie le vie aeree. È utile ricordare che un ambiente nel quale si fuma rappresenta un grave stimolo irritativo per le vie respiratorie e di conseguenza provoca la tosse. In una revisione sistematica della letteratura sulla storia naturale delle infezioni delle prime vie aeree in età pediatrica ad una settimana dall'inizio dei sintomi, dall'8 all'86% dei bambini ha risolto i propri sintomi33. La maggior parte degli studi disponibili si concentra su due molecole: codeina e destrometorfano. I derivati della codeina non inibiscono completamente la tosse neanche negli adulti e, come già accennato, possono avere gravi effetti collaterali specie se assunti in dose eccessiva. Il destrometorfano, che è un analogo dei narcotici, ha un effetto simile alla codeina negli adulti, ma ad alte dosi può causare depressione respiratoria.
Recentemente l'American Academy of Pediatrics ha ribadito quanto espresso in uno statement di circa 10 anni fa nel quale sottolineava che l'efficacia di molecole come codeina e destrometorfano è dimostrata negli adulti ma non nell'età pediatrica e che tali molecole espongono a potenziali effetti collaterali34. Una revisione sistematica più recente conferma la scarsa qualità delle evidenze a disposizione e l'assenza di prove circa l'efficacia di queste molecole per la sedazione della tosse35. Dello stesso tenore una ulteriore revisione sistematica che è stata in grado di selezionare un solo studio di efficacia dei sedativi della tosse senza differenze del gruppo dei trattati rispetto al placebo36. Da una revisione sistematica riguardo all'uso dei beta-2 stimolanti nella bronchite acuta non è emerso inoltre alcun vantaggio dell'albuterolo nel controllo di questo sintomo ed anzi si mostrava una debole associazione con l'occorrenza di tremori37. Per tutte le altre molecole presenti in commercio anche in dosaggio pediatrico, non sono disponibili evidenze derivate da studi condotti su bambini tali da consentire la formulazione di raccomandazioni per il loro uso.
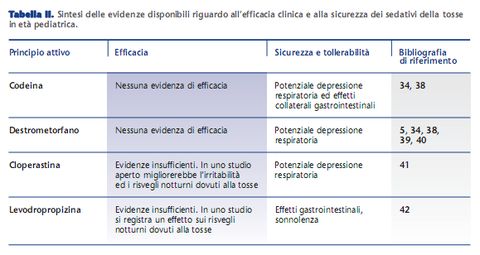
Schematicamente le evidenze a disposizione per questa classe di farmaci sono riassunte nella tabella II. È interessante notare che un recente studio randomizzato in doppio cieco documenta un effetto positivo del miele per la sedazione della tosse notturna. L'uso di questo presidio potrebbe essere considerato alla luce dell'assenza di effetti collaterali associati. La somministrazione di miele va comunque sempre considerata con prudenza, specie nel lattante, per la possibile contaminazione con spore di Clostridium botulinum.
Mucolitici/espettoranti
Il ricorso all'uso dei mucolitici durante le infezioni delle vie aeree superiori in pediatria è particolarmente frequente e probabilmente favorito dalla percezione che questa classe di farmaci non è associata a significativi effetti collaterali. Anche per questa categoria di farmaci gli studi in età pediatrica sono rari e di qualità non sufficiente a permettere una chiara interpretazione dei dati. Un trial randomizzato che aveva studiato l'efficacia della letosteina ha dimostrato un miglioramento dello score clinico nel bambino con infezione respiratoria43. Una revisione sull'efficacia dei mucolitici durante la polmonite acuta nel bambino non è riuscita a dimostrare effetti benefici della bromexina e dell'ambroxolo44. Non esistono altri dati sull'efficacia e la tollerabilità di questa categoria di farmaci in pediatria. Tuttavia sono stati segnalati casi di effetti collaterali a carico del SNC, della cute, della serie piastrinica e dell'apparato gastrointestinale45. Antistaminici
L'istamina secreta nel naso dalle mast cellule e dai basofili è un importante mediatore delle reazioni allergiche; la presenza di allergeni nelle vie aeree causa il rilascio di istamina provocando rinorrea, congestione nasale e starnuti46,47. Gli antistaminici anti H1 bloccano questa reazione alleviando, quindi, i sintomi della rinite allergica.
Poiché nelle infezioni acute delle prime vie respiratorie (in particolare nelle infezioni virali) i sintomi sono molto simili, è stato supposto che gli antistaminici potessero indurre un miglioramento della sintomatologia nasale.
Gli antistaminici, singolarmente o in associazione, sono infatti ampiamente utilizzati come sintomatici nelle infezioni delle prime vie aeree, sia per via orale che topica; molte formulazioni sono vendute come farmaci da banco. L'uso di questi farmaci tuttavia non è supportato da evidenze scientifiche sperimentali o cliniche.
In uno studio46 è stata misurata la quantità di istamina nelle secrezioni nasali in pazienti sperimentalmente infettati da rinovirus senza evidenziarne alcun aumento, smentendo così il razionale patogenetico.
Gli antistaminici di prima generazione provocano come effetto collaterale un'azione anticolinergica e sedativa potenzialmente responsabile del miglioramento dei sintomi; tuttavia una revisione sistematica sull'uso degli antistaminici48 nel raffreddore mostra che non c'è nessuna indicazione, per l'assenza di efficacia e la possibilità di effetti collaterali.
In particolare, dalla revisione si evince che per quanto riguarda i bambini con età inferiore a 6 anni la letteratura è molto scarsa. Sono stati identificati solo due trial clinici che includevano un totale di 212 bambini con età compresa da 6 mesi a 6 anni49,50. I risultati dei due studi sono conflittuali. Lo studio con popolazione più ampia (54 bambini), metodologicamente ben condotto, non evidenzia alcuna efficacia; il secondo trial, in cui i criteri di inclusione non erano ben definiti, la dimensione del campione era molto piccola e venivano inclusi bambini da 2 a 15 anni, mostra invece un beneficio. Da questi dati gli autori della revisione concludono che non ci sono dati sufficienti che supportino l'uso nei bambini piccoli.
Gli studi che hanno analizzato gli antistaminici in associazione con altri farmaci non hanno evidenziato alcun beneficio; d'altro canto va segnalato che negli USA oltre il 5% delle intossicazioni da farmaci è da attribuire a formulazioni di antistaminici in associazione con decongestionanti, utilizzate per il raffreddore51.
Per quanto riguarda i bambini più grandi (età > 6 anni) e gli adulti, i dati sono controversi. Quando usati in monoterapia non si evidenziano risultati clinicamente rilevanti, non c'è miglioramento dell'ostruzione nasale, né della sintomatologia generale. Gli antistaminici di prima generazione mostrano una riduzione della rinorrea ma, come atteso, hanno effetti collaterali maggiori.
Una certa efficacia è stata evidenziata per i farmaci in associazione. Tuttavia gli autori della revisione invitano ad una cauta interpretazione dei risultati poiché gli studi analizzati presentavano problemi metodologici.
Nonostante i dati che supportano l'uso di questi farmaci siano molto scarsi, è stato stimato che negli USA siano stati venduti 95 milioni di confezioni/anno di farmaci da banco per il raffreddore e la tosse (tra cui gli antistaminici) per l'uso pediatrico52.
Una revisione della Food and Drug Administration53 ha identificato oltre 123 morti in bambini con età < 6 anni, con possibile relazione all'uso di farmaci da banco (anche antistaminici in particolare clorfenilamina, doxilamina, carbinoxamina, quest'ultima non in commercio in Italia, sospesa nel 2006 negli USA in seguito alle segnalazioni). Infine seri effetti collaterali sono stati segnalati per sovradosaggio accidentale, sia per interazione farmaco-farmaco che per ospite-farmaco. Medicina alternativa
In Italia un'indagine ISTAT realizzata nel 2005 ha rilevato che circa 7,9 milioni di persone (13,6% ) hanno utilizzato metodi di cura non convenzionali nei tre anni precedenti l'intervista54. In particolare, il 7% della popolazione ha utilizzato l'omeopatia, il 3,7% la fitoterapia.
• Omeopatici. L'omeopatia parte dall'assunto che una sostanza naturale che in dosi quantitativamente misurabili può provocare un determinato sintomo su di un soggetto sano, una volta diluita in dosi omeopatiche può curare quello stesso sintomo nei soggetti malati che lo presentano ed anzi, secondo gli omeopati, tanto maggiore è la diluizione e tanto maggiore è la potenza del rimedio.
In generale gli studi condotti in questo ambito sono poco robusti e caratterizzati da importanti distorsioni55. Inoltre gli studi condotti sulla popolazione pediatrica sono molto scarsi. Sei grandi metanalisi, condotte su studi clinici omeopatici su argomenti diversi, hanno fornito tutte lo stesso risultato: dopo aver escluso i trial metodologicamente inadeguati e tenendo conto del publication bias, le terapie omeopatiche non hanno prodotto risultati statisticamente più significativi di un placebo56-61. Anche una revisione sistematica ancora più recente e su popolazione esclusivamente pediatrica/adolescenziale, che prendeva in considerazione, tra altre nove patologie, le vegetazioni adenoidee, l'asma e le infezioni delle vie respiratorie superiori, non ha rilevato differenze di efficacia rispetto al placebo62.
Due studi riportano risultati positivi nel trattamento delle infezioni delle alte vie respiratorie con omeopa- tici, ma sono indeboliti dalla mancanza di criteri di inclusione e di metodi chiari. Uno è uno studio com- parativo di coorte, multicentrico, non randomizzato, effettuato su 1577 pazienti (adulti e bambini) con sintomi come raffreddore, mal di gola, dolore all'orecchio, ai seni paranasali o tosse da almeno sette giorni, in cui il gruppo che faceva omeopatia è migliorato più rapidamente nella prima settimana dopo il trattamento (sia bambini, che adulti), rispetto al gruppo che faceva terapia convenzionale63.
L'altro è uno studio randomizzato controllato in doppio cieco vs placebo sulla efficacia e sicurezza di una combinazione di rimedi omeopatici per il trattamento delle rinosinusiti acute, effettuato su 144 pa- zienti, in cui il trattamento omeopatico ha portato alla eliminazione dei sintomi nel 90,3% dei pazienti e ad un miglioramento in un ulteriore 8,3%, mentre nel gruppo placebo i sintomi sono rimasti invariati o sono peggiorati nell'88,9% dei pazienti64.
Vi sono anche studi che paragonano l'efficacia clinica degli omeopatici vs antibiotici. In particolare uno studio confronta due strategie di trattamento (terapia omeopatica vs terapia antibiotica) usate nella pratica medica sia da medici generalisti tradizionali che da omeopati nel trattamento della rinofaringite ricorrente. Gli autori concludono che l'omeopatia può essere una alternativa costo-efficace agli antibiotici nel trattamento della rinofaringite ricorrente del bambino, ma si tratta di una analisi retrospettiva, propter hoc, dichiaratamente sponsorizzata65 in quanto realizzata dalla più grande produttrice di omeopatici in Europa.
Anche se si volesse sostenere l'uso della omeopatia come alternativa alla prescrizione inappropriata di antibiotici per patologie respiratorie virali, che secondo una valutazione dei CDC si aggira intorno al 20-50% dei casi tra i medici ambulatoriali americani, ed è responsabile delle crescenti resistenze antibiotiche66, è francamente sconsigliabile ricorrere a terapie alternative la cui efficacia e sicurezza non sono sicuramente provate.
Peraltro considerando che molti pazienti pediatrici, con le loro famiglie, fanno comunque ricorso alla omeopatia, spesso senza nemmeno informarne i loro medici, è importante essere consci di questa eventualità, essere aggiornati sui risultati della ricerca scientifica in questo ambito ed essere aperti alla discussione con i propri pazienti. La valutazione del beneficio in questo tipo di scelta dovrebbe considerare la sicurezza, l'efficacia, il tipo di patologia trattata, le opinioni e le preferenze del paziente e della sua famiglia. L'obiettivo è cercare di condividere con il proprio paziente un livello accettabile di efficacia e sicurezza, che possa consentire l'eventuale uso di questi prodotti67. • Fitoterapici. La fitoterapia è una medicina complementare basata sugli stessi principi scientifici della medicina tradizionale, che fa uso di composti chimici naturali, dotati di attività specifica (piante officinali), in dosi quantitativamente misurabili, e che consente di trattare alcune patologie di entità lieve o moderata.
L'uso inappropriato di antibiotici per le infezioni delle alte vie respiratorie ha portato ad un interesse crescente per nuovi trattamenti, ma sono ancora troppo pochi gli studi robusti e di buona qualità metodologica che sarebbero necessari per validare l'efficacia e la sicurezza delle fitomedicine, soprattutto in età pediatrica. Inoltre la maggior parte delle fitomedicine in commercio è venduta come integratore alimentare, senza essere sottoposta alle verifiche di qualità, sicurezza ed efficacia previste per i farmaci. Sulla confezione di questi integratori spesso non vengono dichiarati componenti, qualità, quantità (titolo) e provenienza. Il prodotto "naturale" viene vissuto come buono, non potenzialmente dannoso, non "farmaco" e quindi utilizzabile senza precisi consigli o prescrizioni mediche; ne consegue che l'utilizzo dei fitoterapici è spesso frutto di una scelta personale, col rischio di un uso non corretto dei prodotti in commercio, per errori nella scelta del farmaco, per dosaggio o modo d'impiego errati, per associazioni farmacologiche impreviste68,69.
Le sostanze fitoterapiche su cui ci sono più studi nel trattamento delle infezioni delle vie aeree superiori (URTI) sono l'echinacea, lo zinco, il geranio sudafricano, l'aglio, l'Andrographis paniculata e l'edera.
Tutte queste sostanze richiedono che siano fatti ulteriori studi perché possano essere raccomandate nella prevenzione e nel trattamento delle infezioni delle alte vie respiratorie, tuttavia su alcune c'è più evidenza di beneficio rispetto ad altre.
Aglio (Allium sativum): le prove finora disponibili non sono sufficienti per raccomandarne l'uso70,71, e rilevano un certo rischio di effetti avversi e reazioni allergiche72.
Kalmegh (Andrographis paniculatae): arbusto le cui foglie vengono usate nella medicina ayurvedica per varie indicazioni, A. paniculata risulta più efficace del placebo nel ridurre i sintomi soggettivi delle infezioni non complicate delle vie respiratorie superiori negli adulti e con effetti avversi lievi e rari73-75, ma le informazioni non sono sufficienti a raccomandarlo, perché gli studi sono su follow-up troppo brevi e su piccoli campioni76-78.
Edera (Hedera helix): la Commissione Tedesca sulla Fitoterapia ne ha approvato l'uso come sintomatico per le infiammazioni respiratorie acute e croniche, e una revisione di 3 studi clinici controllati e randomizzati (RCT) sulla sua efficacia nei bambini con bronchite cronica79 ha rilevato un miglioramento della funzionalità respiratoria (pletismografia e spirometria) rispetto al placebo. Si tratta però di 3 studi soltanto e di scarsa qualità metodologica.
Per saperne di più: http://content.herbalgram.org/bodywise/HerbalMedicine/default.asp?m=53
Echinacea: è una delle droghe vegetali più usate e più studiate, tanto che la spesa per l'echinacea negli USA ha superato i 300 milioni di dollari all'anno80. Tuttavia la sua efficacia terapeutica nel trattamento delle infezioni respiratorie delle prime vie non è ancora chiaramente definita: una Revisione Sistematica Cochrane81 sulla efficacia nel trattamento e prevenzione delle infezioni delle prime vie respiratorie su adulti (16 studi, 22 paragoni) conclude che è importante che consumatori e medici facciano attenzione alla grande variabilità tra i diversi prodotti commerciali di echinacea, che nella stragrande maggioranza dei casi non sono stati testati in studi clinici; l'uso di Echinacea Purpurea ha dimostrato una certa efficacia e potrebbe essere utile nel trattamento precoce del raffreddore negli adulti, ma i risultati non sono completamente coerenti; gli effetti benefici rilevati negli studi che hanno fatto uso di preparazioni di altre varietà di echinacea non sono stati replicati in maniera indipendente in ulteriori trial randomizzati rigorosi. Inoltre non ci sono dati sugli effetti durante l'uso prolungato. Gli effetti avversi più rilevanti sono le reazioni allergiche: in uno studio pediatrico è stato rilevato un incremento assoluto di rash del 5%. Pochi sono gli studi clinici effettuati sulla sua efficacia e sicurezza in età pediatrica ed i risultati, ancor più che in quelli sugli adulti, sono incoerenti: alcuni trial in genere su piccoli numeri hanno dimostrato una certa efficacia82, altri in genere su numeri più ampi, non ne hanno dimostrata alcuna83. Pertanto non ci sono prove sufficienti per suggerire l'uso di echinacea, soprattutto in età pediatrica84,85.
Geranio sudafricano (Umckaloabo, Pelargonium sidoides): le sue radici sono usate nella medicina tradizionale sud africana per il trattamento delle infezioni delle vie respiratorie. Di recente interesse in Europa, soprattutto in Germania, dove il suo estratto attivo EPs7630 è stato registrato nel 2005 con questa indicazione86. Una recente revisione sistematica su 6 RCT di buona qualità, con metanalisi su 4 RCT, sulla efficacia di P. sidoides nel trattamento delle bronchiti acute vs placebo o vs un trattamento convenzionale non antibiotico giunge alla conclusione che ci sono prove di efficacia incoraggianti per il P. sidoides87. Gli studi sui bambini sono meno conclusivi ma incoraggianti, con eventi avversi secondari e transitori88 e con miglioramento o risoluzione clinica dei sintomi respiratori88-90. Tuttavia gli studi disponibili non permettono di raccomandare P. sidoides, perché troppo poco numerosi e di qualità non elevata.
Zinco: è un micronutriente essenziale per la crescita staturo-ponderale e per una adeguata funzione immunitaria. Una recente metanalisi degli RCT sul ruolo dello zinco nella prevenzione di malattie respiratorie e diarrea in bambini di età inferiore ai 5 anni ha selezionato 17 studi e conclude che la supplementazione di zinco riduce significativamente la frequenza e la gravità delle infezioni delle vie respiratorie, ma sono necessari studi più ampi, meno eterogenei e di migliore qualità per identificare le sottopopolazioni che potrebbero averne maggiore beneficio91. Per quanto riguarda gli studi sullo zinco ed il raffreddore comune, questi sono molto meno numerosi, meno robusti e di minore qualità. Alcuni studi danno risultati di modesta efficacia nel trattamento del raffreddore con zinco91,93, altri di nessuna efficacia rispetto al placebo94. È stato riportato che lo zinco per spray nasale (orotato o gluconato) può produrre anosmia potenzialmente permanente95. Lo zinco gluconato non sembra avere effetti sulla gravità dei sintomi e lo zinco acetato non sembra avere effetti sulla gravità e sulla durata dei sintomi del raffreddore comune. I preparati a base di zinco sembrano in buona sostanza di scarsa utilità per il trattamento del raffreddore comune96. La revisione di sette revisioni sistematiche Cochrane sul trattamento non antibiotico del "common cold" ha rilevato che un tema comune è l'estrema variabilità della qualità degli studi primari e conclude che la maggior parte dei trattamenti alternativi per il raffreddore comune probabilmente non sono efficaci97.
Una revisione98 delle prove di efficacia e sicurezza delle medicine non convenzionali nel trattamento e prevenzione delle infezioni delle alte vie respiratorie in età pediatrica ha esaminato i lavori pubblicati fino al 2005, selezionandone 6 sulle fitomedicine e 9 riguardanti altre terapie alternative/complementari, in base all'aderenza a criteri standard di efficacia e sicurezza, ed ha rilevato che:
L'uso dei farmaci per il trattamento di supporto delle infezioni delle vie respiratorie in pediatria rappresenta una delle pratiche di più frequente ricorso. A fronte della grande popolarità di questi farmaci, le prove di efficacia a loro favore sono frequentemente estrapolate da studi effettuati sugli adulti, e i rari studi disponibili per l'età pediatrica non supportano l'efficacia della maggior parte delle molecole utilizzate per questo scopo. In alcuni casi, inoltre, alcuni principi attivi contenuti nei farmaci per il trattamento di supporto delle infezioni respiratorie sono associati ad effetti collaterali importanti.
Alla luce delle evidenze disponibili, nel bambino con infezione delle vie aeree superiori:
Le infezioni delle prime vie respiratorie sono prevalentemente ad eziologia virale ed includono il raffreddore comune, l'influenza, la laringite, la faringite, la sinusite, la tonsillite ed il croup. Le infezioni delle prime vie aeree rappresentano la causa più frequente di consultazione del pediatra e colpiscono soprattutto i bambini di età inferiore a 2 anni e quelli che frequentano le comunità infantili. Si stima che in media un bimbo nei primi anni di vita abbia più di 4 episodi di infezione delle prime vie aeree1.
Esiste una chiara stagionalità nella circolazione dei virus che sono più frequentemente responsabili di infezioni delle prime vie aeree; in particolare durante l'inverno il virus respiratorio sinciziale, i virus influenzali e i parainfluenzali, gli adenovirus, rinovirus e coronavirus sono i più frequenti agenti eziologici. Più raramente queste infezioni sono sostenute da batteri come lo Streptococcus pneumoniae. Le manifestazioni cliniche di queste infezioni includono sistematicamente congestione e secrezione nasale, starnuti, mal di gola, tosse, malessere generale e febbre. La trasmissione di queste infezioni avviene per via respiratoria attraverso le goccioline di saliva oppure per la contaminazione di superfici e conseguente contatto con le mani. Occasionalmente queste infezioni possono essere seguite da complicazioni batteriche come l'otite media, la sinusite e la polmonite. Talvolta le infezioni delle prime vie aeree possono essere seguite da complicanze anch'esse virali come la bronchiolite, la polmonite o il croup. Le infezioni respiratorie sostenute da virus sono autolimitanti e, sebbene le complicazioni siano un'evenienza rara, data l'elevata frequenza, il loro impatto è notevole sulle prescrizioni farmaceutiche e sul consumo di farmaci da banco. Nonostante queste infezioni procurino sintomi solo per alcuni giorni, e difficilmente oltre una settimana, la presenza dei tipici fastidiosi segni clinici è causa di sistematiche richieste e consumo di farmaci per il loro trattamento.
La gestione delle infezioni respiratorie delle prime vie aeree dovrebbe comprendere i seguenti punti3:
- una buona comunicazione con i genitori per anticipare la tipologia e la durata dei sintomi e rassicurarli sul fatto che questo tipo di infezioni sono nella maggior parte dei casi clinicamente modeste e guariscono spontaneamente;
- un adeguato apporto di liquidi;
- l'uso oculato di farmaci di supporto per il controllo della febbre e degli altri sintomi;
- evitare l'esposizione al fumo passivo.
Alcuni preparati associano parte dei farmaci disponibili per il trattamento dei sintomi delle infezioni delle prime vie aeree con altri farmaci che rendono potenzialmente maggiore il rischio di effetti collaterali. Inoltre, paradossalmente, le prove a favore dell'efficacia di questi trattamenti per la risoluzione dei sintomi nelle affezioni respiratorie sono scarse e, per alcuni di essi, sono semplicemente estrapolate da studi effettuati nella popolazione adulta. Queste osservazioni dovrebbero essere sempre considerate nel processo decisionale per la gestione terapeutica. Antipiretici e antinfiammatori
I farmaci da banco come paracetamolo, ibuprofene ed acido acetilsalicilico (ASA) sono i farmaci più utilizzati nel trattamento sintomatico delle infezioni delle prime vie respiratorie. Nonostante il diffuso utilizzo, c'è poca letteratura per questo specifico uso, sia negli adulti che nei bambini. I dati sono quindi estrapolati da studi sulla febbre o sul dolore. Gli autori di una recente revisione sistematica6 hanno analizzato la letteratura per puntualizzare i dati disponibili in termini di efficacia e di sicurezza.
Il paracetamolo è largamente utilizzato per l'effetto antipiretico e antidolorifico. Le dosi raccomandate sono illustrate nella tabella I.
Per quanto riguarda la sicurezza, in una revisione su 40 anni d'uso del paracetamolo nei bambini7, gli autori concludono che "questa molecola rimane la prima scelta tra i farmaci da banco per l'analgesia e l'antipiresi e che quando utilizzata nelle dosi raccomandate ha pochi effetti collaterali essendo sostanzialmente ben tollerata".
Gli effetti collaterali (epato e nefro tossicità) sono dovuti al sovradosaggio. La dose epatotossica è di 150 mg/kg o 75mg/kg nei bambini con rischio aumentato di sviluppare danno epatico (patologie epatiche, malnutrizione, terapia con induttori enzimatici - carbamazepina, fenobarbital, fenitoina, rifampicina - infezione da HIV, patologie metaboliche).
Sull'efficacia dell'ibuprofene, da qualche anno largamente utilizzato come antipiretico in pediatria, sono disponibili prevalentemente studi clinici comparativi con il paracetamolo piuttosto che contro placebo. Molti di questi studi hanno mostrato una equivalenza di efficacia tra le due molecole, soprattutto come azione antipiretica8,9.
In uno studio clinico randomizzato in doppio cieco condotto su bambini con età compresa tra 2 e 12 anni, una singola dose (10 mg/kg) di ibuprofene si è dimostrata efficace e superiore al placebo sia per il trattamento della faringodinia che della febbre associata ad infezione delle prime vie respiratorie10. Anche per l'ibuprofene i dati sulla sicurezza sono rassicuranti. Due revisioni sistematiche analizzano l'efficacia ma anche la sicurezza del paracetamolo e dell'ibuprofene, con dati positivi per entrambe. Un ampio trial clinico randomizzato condotto su 27.065 bambini febbrili con età inferiore a 2 anni ha studiato la sicurezza di: paracetamolo 12 mg/kg, ibuprofene 5 mg/kg e ibuprofene 10 mg/kg. Gli autori concludono che con questi farmaci il rischio di seri effetti collaterali è basso11,12.
Poiché l'ibuprofene appartiene alla categoria dei farmaci antinfiammatori non steroidei (FANS), non va somministrato nei pazienti con ulcera peptica attiva o con anamnesi positiva o con reazioni di ipersensibilità ai FANS. Tuttavia tra gli antinfiammatori viene considerato il più sicuro in termini di effetti gastrointestinali. La letteratura non indica alcun rischio di danno intestinale o sanguinamento per l'uso di breve durata alle dosi utilizzate come antipiretico13-15.
Sebbene vi siano dei vecchi studi sull'efficacia dell'ASA nei bambini, per il rischio di sindrome di Reye l'ASA è controindicato nei bambini con età inferiore ai 12 anni. La sindrome di Reye è una patologia rara ma a rischio di morte ed è tipicamente associata all'uso di ASA in caso di infezioni virali, soprattutto influenza e varicella16-19. Decongestionanti nasali
La congestione nasale è il sintomo che più frequentemente viene riferito in corso di infezioni delle alte vie aeree. I decongestionanti nasali sono rappresentati da una vasta gamma di principi attivi disponibili singolarmente o in associazione, sia sotto forma di preparazioni per uso topico sia sistemico. Si tratta principalmente di due categorie di sostanze: derivati delle catecolamine (amine simpaticomimetiche quali efedrina, fenilefrina, fenilpropanolamina, tuaminoeptano, p-ossifenilpropilamina iodidrato) e derivati imidazolinici (benzilimidazoline come ossimetazolina, xilometazolina; naftimidazoline come nafazolina, tetrizolina, tramazolina, clonazolina). Questi farmaci hanno varie indicazioni autorizzate (per esempio rinite, faringite acuta e catarrale, otite catarrale, processi infiammatori nasali e paranasali, rinite allergica, sinusite acuta, ecc.), ma sono prescritti, o più spesso autosomministrati, per alleviare i sintomi del raffreddore tra cui l'ostruzione nasale. Il meccanismo di azione è mediato dalla vasocostrizione arteriolare indotta da queste sostanze, mentre non vi è influenza sugli altri meccanismi (edema mucosale, essudazione e secrezione fluida nelle vie aeree) che causano i sintomi.
Una revisione sistematica del 2007 analizza 7 studi sull'adulto riguardanti l'utilizzo di decongestionanti nasali in corso di infezione delle alte vie aeree. Confrontati con placebo, i decongestionanti nasali mostrerebbero un piccolo ma statisticamente significativo miglioramento nel ridurre il sintomo (circa il 6%)20. Non sembrerebbe esserci differenza per quanto concerne l'efficacia nell'utilizzo topico o per via orale.
Negli studi identificati dalla revisione non sono stati indagati o riportati effetti avversi; solo due studi infatti hanno riportato i dati di sicurezza, mostrando un'incidenza di reazioni avverse ai decongestionanti relativamente esigua e un piccolo aumento (5%) del rischio di insonnia, per lo più in concomitanza con l'assunzione di pseudoefedrina20.
Da altri studi è noto comunque che i decongestionanti nasali, soprattutto se usati per periodi superiori a 5 giorni, possono indurre reazioni avverse a livello locale, generalmente irritazione locale transitoria; la vasocostrizione indotta dai decongestionanti topici può però essere seguita da vasodilatazione o congestione rebound, che sembra essere meno marcata per i derivati imidazolinici e per l'ossifenil-propilamina iodioidrato. Il paziente, se non avvertito, pensando di sopperire alla ridotta efficacia tende ad incrementare la dose e la frequenza delle somministrazioni per ottenere sollievo dalla congestione secondaria, ignorando che quest'ultima è indotta dallo stesso farmaco.
Nel tempo la ridotta sensibilità dei recettori alfa adrenergici può causare tachifilassi. Per questo motivo il trattamento non deve durare più di 2-5 giorni. L'abuso dei vasocostrittori, indotto dal fenomeno della congestione rebound e della tachifilassi, e lo scorretto uso del farmaco possono determinare alterazioni prolungate della mucosa che risultano in rinite atrofica medicamentosa. Poiché la mucosa nasale è una buona superficie di assorbimento, in circostanze rare quantità significative di questi farmaci possono essere assorbite e causare a livello sistemico effetti simpaticomimetici. Le reazioni avverse più significative sono a carico dell'apparato cardiovascolare (ipertensione arteriosa, tachicardia, pallore, sudorazione, bradicardia, ipotensione arteriosa) e del sistema nervoso centrale - SNC (cefalea, depressione neurologica con sintomi che vanno dalla sonnolenza fino al coma e depressione respiratoria).
Nonostante l'elevata incidenza di raffreddore nei bambini, non sono stati identificati trial sui decongestionanti nasali utilizzati al di sotto dei 12 anni di età che rispondevano ai criteri di inclusione della revisione.
Due trial randomizzati in doppio cieco con placebo che includevano l'utilizzo di antistaminici e decongestionanti in combinazione in bambini da 6 mesi a 5 anni non hanno identificato differenze significative nella durata e nella gravità dei sintomi21,22.
Le differenze esistenti tra la popolazione adulta e quella pediatrica, sia nell'anatomia nasale sia nella tolleranza ai farmaci, non permettono un'estrapolazione dell'efficacia e della sicurezza dei decongestionanti nei bambini.
Nella Rete Nazionale di Farmacovigilanza sono inoltre presenti alcune segnalazioni di reazioni avverse associate a farmaci simpaticomimetici per uso topico, analogamente a quanto avviene a livello internazionale23-25. Riguardano soprattutto bambini molto piccoli (al di sotto di 1 anno e tra 1 e 3 anni), sono gravi e prevalentemente a carico della cute e del tessuto sottocutaneo (reazioni da ipersensibilità, prurito, eritema, edema faringeo, orticaria, sudorazione, necrolisi epidermica, esantema eritematoso), del SNC (ipotonia, torpore, contrazioni muscolari involontarie, pallore, agitazione, sonnolenza, ipercinesia, irritabilità, depressione, letargia), della mucosa nasale (rinite medicamentosa), dell'apparato cardiovascolare (extrasistoli, vasodilatazione, tachicardia, bradicardia), dell'apparato respiratorio (depressione respiratoria, dispnea, apnea, broncospasmo).
A tal proposito nel 2000 la European Accademy of Allergology and Clinical Immunology ha pubblicato il "Consensus statement on treatment of allergic rhinitis" in cui non si raccomanda l'uso di decongestionanti nasali nei bambini molto piccoli a causa dei possibili effetti collaterali e dello stretto range tra la dose terapeutica e quella tossica26.
La maggior parte delle specialità in commercio non è stata testata su pazienti pediatrici, quindi questi prodotti vengono utilizzati off-label ricorrendo, per i dosaggi, all'estrapolazione di dosaggi calcolati per adulti. I bambini quindi rappresentano una popolazione ad alto rischio per le possibili complicanze da sovradosaggio.
I Centers for Disease Control and Prevention (CDC) della Food and Drug Administration hanno indagato sul decesso di tre bambini di età compresa tra 1 e 6 mesi, la cui morte è stata imputata alle altissime concentrazioni di pseudoefedrina plasmatica, e dall'analisi effettuata è emerso che, durante il 2004 e 2005, più di 1500 bambini sono stati ricoverati negli ospedali americani per gli effetti avversi legati ai farmaci per tosse e raffreddore, sovradosaggio compreso. Questi prodotti possono comunque essere acquistati senza ricetta sia in USA che in Europa.
La rivalutazione del profilo beneficio/rischio di questi farmaci nei bambini ha dato esito sfavorevole, pertanto l'Agenzia Italiana del Farmaco ha adottato un provvedimento restrittivo vietando l'uso dei decongestionanti nasali ad attività simpaticomimetica nei bambini al di sotto di 12 anni27. Farmaci per via inalatoria: la terapia aerosolica
Respirare vapore o aria calda è generalmente considerato un aiuto privo di effetti collaterali per trattare la congestione nasale e sinusale. Il beneficio fisico è verosimilmente legato alla liquefazione delle secrezioni respiratorie che permette una rimozione più efficace mediante la tosse o soffiandosi il naso; inoltre si apprezza un effetto lenitivo sulle mucose.
Esistono alcuni studi che hanno tentato di valutare l'effetto dell'inalazione con vapore nel raffreddore comune, tutti condotti su pazienti adulti, che hanno dato risultati contrastanti28-30.
Tenuto anche conto della difficoltà ad eseguire una terapia aerosolica ad un bambino e vista la scarsità delle evidenze per sostenere tale indicazione, non è da considerarsi un trattamento risolutivo. L'utilizzo di ribavirina o antibiotici per via aerosolica è segnalato in categorie di pazienti a rischio e pertanto non è da considerarsi una pratica routinaria31,32. Non esistono studi che valutino l'efficacia e la tollerabilità di steroidi per via inalatoria negli episodi respiratori acuti delle vie aeree superiori che non siano associati ad asma o wheezing. Sedativi della tosse
L'uso dei sedativi della tosse nelle affezioni delle prime vie aeree in età pediatrica è controverso e largamente basato sull'estrapolazione di studi clinici effettuati negli adulti. La tosse è un meccanismo fisiologico di protezione che ha lo scopo di eliminare le secrezioni dell'albero respiratorio e di mantenere pervie le vie aeree. È utile ricordare che un ambiente nel quale si fuma rappresenta un grave stimolo irritativo per le vie respiratorie e di conseguenza provoca la tosse. In una revisione sistematica della letteratura sulla storia naturale delle infezioni delle prime vie aeree in età pediatrica ad una settimana dall'inizio dei sintomi, dall'8 all'86% dei bambini ha risolto i propri sintomi33. La maggior parte degli studi disponibili si concentra su due molecole: codeina e destrometorfano. I derivati della codeina non inibiscono completamente la tosse neanche negli adulti e, come già accennato, possono avere gravi effetti collaterali specie se assunti in dose eccessiva. Il destrometorfano, che è un analogo dei narcotici, ha un effetto simile alla codeina negli adulti, ma ad alte dosi può causare depressione respiratoria.
Recentemente l'American Academy of Pediatrics ha ribadito quanto espresso in uno statement di circa 10 anni fa nel quale sottolineava che l'efficacia di molecole come codeina e destrometorfano è dimostrata negli adulti ma non nell'età pediatrica e che tali molecole espongono a potenziali effetti collaterali34. Una revisione sistematica più recente conferma la scarsa qualità delle evidenze a disposizione e l'assenza di prove circa l'efficacia di queste molecole per la sedazione della tosse35. Dello stesso tenore una ulteriore revisione sistematica che è stata in grado di selezionare un solo studio di efficacia dei sedativi della tosse senza differenze del gruppo dei trattati rispetto al placebo36. Da una revisione sistematica riguardo all'uso dei beta-2 stimolanti nella bronchite acuta non è emerso inoltre alcun vantaggio dell'albuterolo nel controllo di questo sintomo ed anzi si mostrava una debole associazione con l'occorrenza di tremori37. Per tutte le altre molecole presenti in commercio anche in dosaggio pediatrico, non sono disponibili evidenze derivate da studi condotti su bambini tali da consentire la formulazione di raccomandazioni per il loro uso.
Schematicamente le evidenze a disposizione per questa classe di farmaci sono riassunte nella tabella II. È interessante notare che un recente studio randomizzato in doppio cieco documenta un effetto positivo del miele per la sedazione della tosse notturna. L'uso di questo presidio potrebbe essere considerato alla luce dell'assenza di effetti collaterali associati. La somministrazione di miele va comunque sempre considerata con prudenza, specie nel lattante, per la possibile contaminazione con spore di Clostridium botulinum.
Mucolitici/espettoranti
Il ricorso all'uso dei mucolitici durante le infezioni delle vie aeree superiori in pediatria è particolarmente frequente e probabilmente favorito dalla percezione che questa classe di farmaci non è associata a significativi effetti collaterali. Anche per questa categoria di farmaci gli studi in età pediatrica sono rari e di qualità non sufficiente a permettere una chiara interpretazione dei dati. Un trial randomizzato che aveva studiato l'efficacia della letosteina ha dimostrato un miglioramento dello score clinico nel bambino con infezione respiratoria43. Una revisione sull'efficacia dei mucolitici durante la polmonite acuta nel bambino non è riuscita a dimostrare effetti benefici della bromexina e dell'ambroxolo44. Non esistono altri dati sull'efficacia e la tollerabilità di questa categoria di farmaci in pediatria. Tuttavia sono stati segnalati casi di effetti collaterali a carico del SNC, della cute, della serie piastrinica e dell'apparato gastrointestinale45. Antistaminici
L'istamina secreta nel naso dalle mast cellule e dai basofili è un importante mediatore delle reazioni allergiche; la presenza di allergeni nelle vie aeree causa il rilascio di istamina provocando rinorrea, congestione nasale e starnuti46,47. Gli antistaminici anti H1 bloccano questa reazione alleviando, quindi, i sintomi della rinite allergica.
Poiché nelle infezioni acute delle prime vie respiratorie (in particolare nelle infezioni virali) i sintomi sono molto simili, è stato supposto che gli antistaminici potessero indurre un miglioramento della sintomatologia nasale.
Gli antistaminici, singolarmente o in associazione, sono infatti ampiamente utilizzati come sintomatici nelle infezioni delle prime vie aeree, sia per via orale che topica; molte formulazioni sono vendute come farmaci da banco. L'uso di questi farmaci tuttavia non è supportato da evidenze scientifiche sperimentali o cliniche.
In uno studio46 è stata misurata la quantità di istamina nelle secrezioni nasali in pazienti sperimentalmente infettati da rinovirus senza evidenziarne alcun aumento, smentendo così il razionale patogenetico.
Gli antistaminici di prima generazione provocano come effetto collaterale un'azione anticolinergica e sedativa potenzialmente responsabile del miglioramento dei sintomi; tuttavia una revisione sistematica sull'uso degli antistaminici48 nel raffreddore mostra che non c'è nessuna indicazione, per l'assenza di efficacia e la possibilità di effetti collaterali.
In particolare, dalla revisione si evince che per quanto riguarda i bambini con età inferiore a 6 anni la letteratura è molto scarsa. Sono stati identificati solo due trial clinici che includevano un totale di 212 bambini con età compresa da 6 mesi a 6 anni49,50. I risultati dei due studi sono conflittuali. Lo studio con popolazione più ampia (54 bambini), metodologicamente ben condotto, non evidenzia alcuna efficacia; il secondo trial, in cui i criteri di inclusione non erano ben definiti, la dimensione del campione era molto piccola e venivano inclusi bambini da 2 a 15 anni, mostra invece un beneficio. Da questi dati gli autori della revisione concludono che non ci sono dati sufficienti che supportino l'uso nei bambini piccoli.
Gli studi che hanno analizzato gli antistaminici in associazione con altri farmaci non hanno evidenziato alcun beneficio; d'altro canto va segnalato che negli USA oltre il 5% delle intossicazioni da farmaci è da attribuire a formulazioni di antistaminici in associazione con decongestionanti, utilizzate per il raffreddore51.
Per quanto riguarda i bambini più grandi (età > 6 anni) e gli adulti, i dati sono controversi. Quando usati in monoterapia non si evidenziano risultati clinicamente rilevanti, non c'è miglioramento dell'ostruzione nasale, né della sintomatologia generale. Gli antistaminici di prima generazione mostrano una riduzione della rinorrea ma, come atteso, hanno effetti collaterali maggiori.
Una certa efficacia è stata evidenziata per i farmaci in associazione. Tuttavia gli autori della revisione invitano ad una cauta interpretazione dei risultati poiché gli studi analizzati presentavano problemi metodologici.
Nonostante i dati che supportano l'uso di questi farmaci siano molto scarsi, è stato stimato che negli USA siano stati venduti 95 milioni di confezioni/anno di farmaci da banco per il raffreddore e la tosse (tra cui gli antistaminici) per l'uso pediatrico52.
Una revisione della Food and Drug Administration53 ha identificato oltre 123 morti in bambini con età < 6 anni, con possibile relazione all'uso di farmaci da banco (anche antistaminici in particolare clorfenilamina, doxilamina, carbinoxamina, quest'ultima non in commercio in Italia, sospesa nel 2006 negli USA in seguito alle segnalazioni). Infine seri effetti collaterali sono stati segnalati per sovradosaggio accidentale, sia per interazione farmaco-farmaco che per ospite-farmaco. Medicina alternativa
In Italia un'indagine ISTAT realizzata nel 2005 ha rilevato che circa 7,9 milioni di persone (13,6% ) hanno utilizzato metodi di cura non convenzionali nei tre anni precedenti l'intervista54. In particolare, il 7% della popolazione ha utilizzato l'omeopatia, il 3,7% la fitoterapia.
• Omeopatici. L'omeopatia parte dall'assunto che una sostanza naturale che in dosi quantitativamente misurabili può provocare un determinato sintomo su di un soggetto sano, una volta diluita in dosi omeopatiche può curare quello stesso sintomo nei soggetti malati che lo presentano ed anzi, secondo gli omeopati, tanto maggiore è la diluizione e tanto maggiore è la potenza del rimedio.
In generale gli studi condotti in questo ambito sono poco robusti e caratterizzati da importanti distorsioni55. Inoltre gli studi condotti sulla popolazione pediatrica sono molto scarsi. Sei grandi metanalisi, condotte su studi clinici omeopatici su argomenti diversi, hanno fornito tutte lo stesso risultato: dopo aver escluso i trial metodologicamente inadeguati e tenendo conto del publication bias, le terapie omeopatiche non hanno prodotto risultati statisticamente più significativi di un placebo56-61. Anche una revisione sistematica ancora più recente e su popolazione esclusivamente pediatrica/adolescenziale, che prendeva in considerazione, tra altre nove patologie, le vegetazioni adenoidee, l'asma e le infezioni delle vie respiratorie superiori, non ha rilevato differenze di efficacia rispetto al placebo62.
Due studi riportano risultati positivi nel trattamento delle infezioni delle alte vie respiratorie con omeopa- tici, ma sono indeboliti dalla mancanza di criteri di inclusione e di metodi chiari. Uno è uno studio com- parativo di coorte, multicentrico, non randomizzato, effettuato su 1577 pazienti (adulti e bambini) con sintomi come raffreddore, mal di gola, dolore all'orecchio, ai seni paranasali o tosse da almeno sette giorni, in cui il gruppo che faceva omeopatia è migliorato più rapidamente nella prima settimana dopo il trattamento (sia bambini, che adulti), rispetto al gruppo che faceva terapia convenzionale63.
L'altro è uno studio randomizzato controllato in doppio cieco vs placebo sulla efficacia e sicurezza di una combinazione di rimedi omeopatici per il trattamento delle rinosinusiti acute, effettuato su 144 pa- zienti, in cui il trattamento omeopatico ha portato alla eliminazione dei sintomi nel 90,3% dei pazienti e ad un miglioramento in un ulteriore 8,3%, mentre nel gruppo placebo i sintomi sono rimasti invariati o sono peggiorati nell'88,9% dei pazienti64.
Vi sono anche studi che paragonano l'efficacia clinica degli omeopatici vs antibiotici. In particolare uno studio confronta due strategie di trattamento (terapia omeopatica vs terapia antibiotica) usate nella pratica medica sia da medici generalisti tradizionali che da omeopati nel trattamento della rinofaringite ricorrente. Gli autori concludono che l'omeopatia può essere una alternativa costo-efficace agli antibiotici nel trattamento della rinofaringite ricorrente del bambino, ma si tratta di una analisi retrospettiva, propter hoc, dichiaratamente sponsorizzata65 in quanto realizzata dalla più grande produttrice di omeopatici in Europa.
Anche se si volesse sostenere l'uso della omeopatia come alternativa alla prescrizione inappropriata di antibiotici per patologie respiratorie virali, che secondo una valutazione dei CDC si aggira intorno al 20-50% dei casi tra i medici ambulatoriali americani, ed è responsabile delle crescenti resistenze antibiotiche66, è francamente sconsigliabile ricorrere a terapie alternative la cui efficacia e sicurezza non sono sicuramente provate.
Peraltro considerando che molti pazienti pediatrici, con le loro famiglie, fanno comunque ricorso alla omeopatia, spesso senza nemmeno informarne i loro medici, è importante essere consci di questa eventualità, essere aggiornati sui risultati della ricerca scientifica in questo ambito ed essere aperti alla discussione con i propri pazienti. La valutazione del beneficio in questo tipo di scelta dovrebbe considerare la sicurezza, l'efficacia, il tipo di patologia trattata, le opinioni e le preferenze del paziente e della sua famiglia. L'obiettivo è cercare di condividere con il proprio paziente un livello accettabile di efficacia e sicurezza, che possa consentire l'eventuale uso di questi prodotti67. • Fitoterapici. La fitoterapia è una medicina complementare basata sugli stessi principi scientifici della medicina tradizionale, che fa uso di composti chimici naturali, dotati di attività specifica (piante officinali), in dosi quantitativamente misurabili, e che consente di trattare alcune patologie di entità lieve o moderata.
L'uso inappropriato di antibiotici per le infezioni delle alte vie respiratorie ha portato ad un interesse crescente per nuovi trattamenti, ma sono ancora troppo pochi gli studi robusti e di buona qualità metodologica che sarebbero necessari per validare l'efficacia e la sicurezza delle fitomedicine, soprattutto in età pediatrica. Inoltre la maggior parte delle fitomedicine in commercio è venduta come integratore alimentare, senza essere sottoposta alle verifiche di qualità, sicurezza ed efficacia previste per i farmaci. Sulla confezione di questi integratori spesso non vengono dichiarati componenti, qualità, quantità (titolo) e provenienza. Il prodotto "naturale" viene vissuto come buono, non potenzialmente dannoso, non "farmaco" e quindi utilizzabile senza precisi consigli o prescrizioni mediche; ne consegue che l'utilizzo dei fitoterapici è spesso frutto di una scelta personale, col rischio di un uso non corretto dei prodotti in commercio, per errori nella scelta del farmaco, per dosaggio o modo d'impiego errati, per associazioni farmacologiche impreviste68,69.
Le sostanze fitoterapiche su cui ci sono più studi nel trattamento delle infezioni delle vie aeree superiori (URTI) sono l'echinacea, lo zinco, il geranio sudafricano, l'aglio, l'Andrographis paniculata e l'edera.
Tutte queste sostanze richiedono che siano fatti ulteriori studi perché possano essere raccomandate nella prevenzione e nel trattamento delle infezioni delle alte vie respiratorie, tuttavia su alcune c'è più evidenza di beneficio rispetto ad altre.
Aglio (Allium sativum): le prove finora disponibili non sono sufficienti per raccomandarne l'uso70,71, e rilevano un certo rischio di effetti avversi e reazioni allergiche72.
Kalmegh (Andrographis paniculatae): arbusto le cui foglie vengono usate nella medicina ayurvedica per varie indicazioni, A. paniculata risulta più efficace del placebo nel ridurre i sintomi soggettivi delle infezioni non complicate delle vie respiratorie superiori negli adulti e con effetti avversi lievi e rari73-75, ma le informazioni non sono sufficienti a raccomandarlo, perché gli studi sono su follow-up troppo brevi e su piccoli campioni76-78.
Edera (Hedera helix): la Commissione Tedesca sulla Fitoterapia ne ha approvato l'uso come sintomatico per le infiammazioni respiratorie acute e croniche, e una revisione di 3 studi clinici controllati e randomizzati (RCT) sulla sua efficacia nei bambini con bronchite cronica79 ha rilevato un miglioramento della funzionalità respiratoria (pletismografia e spirometria) rispetto al placebo. Si tratta però di 3 studi soltanto e di scarsa qualità metodologica.
Per saperne di più: http://content.herbalgram.org/bodywise/HerbalMedicine/default.asp?m=53
Echinacea: è una delle droghe vegetali più usate e più studiate, tanto che la spesa per l'echinacea negli USA ha superato i 300 milioni di dollari all'anno80. Tuttavia la sua efficacia terapeutica nel trattamento delle infezioni respiratorie delle prime vie non è ancora chiaramente definita: una Revisione Sistematica Cochrane81 sulla efficacia nel trattamento e prevenzione delle infezioni delle prime vie respiratorie su adulti (16 studi, 22 paragoni) conclude che è importante che consumatori e medici facciano attenzione alla grande variabilità tra i diversi prodotti commerciali di echinacea, che nella stragrande maggioranza dei casi non sono stati testati in studi clinici; l'uso di Echinacea Purpurea ha dimostrato una certa efficacia e potrebbe essere utile nel trattamento precoce del raffreddore negli adulti, ma i risultati non sono completamente coerenti; gli effetti benefici rilevati negli studi che hanno fatto uso di preparazioni di altre varietà di echinacea non sono stati replicati in maniera indipendente in ulteriori trial randomizzati rigorosi. Inoltre non ci sono dati sugli effetti durante l'uso prolungato. Gli effetti avversi più rilevanti sono le reazioni allergiche: in uno studio pediatrico è stato rilevato un incremento assoluto di rash del 5%. Pochi sono gli studi clinici effettuati sulla sua efficacia e sicurezza in età pediatrica ed i risultati, ancor più che in quelli sugli adulti, sono incoerenti: alcuni trial in genere su piccoli numeri hanno dimostrato una certa efficacia82, altri in genere su numeri più ampi, non ne hanno dimostrata alcuna83. Pertanto non ci sono prove sufficienti per suggerire l'uso di echinacea, soprattutto in età pediatrica84,85.
Geranio sudafricano (Umckaloabo, Pelargonium sidoides): le sue radici sono usate nella medicina tradizionale sud africana per il trattamento delle infezioni delle vie respiratorie. Di recente interesse in Europa, soprattutto in Germania, dove il suo estratto attivo EPs7630 è stato registrato nel 2005 con questa indicazione86. Una recente revisione sistematica su 6 RCT di buona qualità, con metanalisi su 4 RCT, sulla efficacia di P. sidoides nel trattamento delle bronchiti acute vs placebo o vs un trattamento convenzionale non antibiotico giunge alla conclusione che ci sono prove di efficacia incoraggianti per il P. sidoides87. Gli studi sui bambini sono meno conclusivi ma incoraggianti, con eventi avversi secondari e transitori88 e con miglioramento o risoluzione clinica dei sintomi respiratori88-90. Tuttavia gli studi disponibili non permettono di raccomandare P. sidoides, perché troppo poco numerosi e di qualità non elevata.
Zinco: è un micronutriente essenziale per la crescita staturo-ponderale e per una adeguata funzione immunitaria. Una recente metanalisi degli RCT sul ruolo dello zinco nella prevenzione di malattie respiratorie e diarrea in bambini di età inferiore ai 5 anni ha selezionato 17 studi e conclude che la supplementazione di zinco riduce significativamente la frequenza e la gravità delle infezioni delle vie respiratorie, ma sono necessari studi più ampi, meno eterogenei e di migliore qualità per identificare le sottopopolazioni che potrebbero averne maggiore beneficio91. Per quanto riguarda gli studi sullo zinco ed il raffreddore comune, questi sono molto meno numerosi, meno robusti e di minore qualità. Alcuni studi danno risultati di modesta efficacia nel trattamento del raffreddore con zinco91,93, altri di nessuna efficacia rispetto al placebo94. È stato riportato che lo zinco per spray nasale (orotato o gluconato) può produrre anosmia potenzialmente permanente95. Lo zinco gluconato non sembra avere effetti sulla gravità dei sintomi e lo zinco acetato non sembra avere effetti sulla gravità e sulla durata dei sintomi del raffreddore comune. I preparati a base di zinco sembrano in buona sostanza di scarsa utilità per il trattamento del raffreddore comune96. La revisione di sette revisioni sistematiche Cochrane sul trattamento non antibiotico del "common cold" ha rilevato che un tema comune è l'estrema variabilità della qualità degli studi primari e conclude che la maggior parte dei trattamenti alternativi per il raffreddore comune probabilmente non sono efficaci97.
Una revisione98 delle prove di efficacia e sicurezza delle medicine non convenzionali nel trattamento e prevenzione delle infezioni delle alte vie respiratorie in età pediatrica ha esaminato i lavori pubblicati fino al 2005, selezionandone 6 sulle fitomedicine e 9 riguardanti altre terapie alternative/complementari, in base all'aderenza a criteri standard di efficacia e sicurezza, ed ha rilevato che:
- l'echinacea non riduce la durata e la gravità di URTI;
- la Andrographis paniculata e l'echinacea riducono le secrezioni nasali (P<0,01) ma non i sintomi di URTI;
- una combinazione di echinacea, propoli ed acido ascorbico ha ridotto il numero di episodi di URTI, la durata dei sintomi ed il numero di giorni di malattia (P<0,001);
- l'uso di echinacea è risultato associato ad una più alta frequenza di rash, rispetto al placebo (P=0,008);
- l'acido ascorbico da solo e la terapia omeopatica non si sono rivelate efficaci;
- l'efficacia dello zinco è controversa e può essere associata ad effetti avversi nei bambini.
L'uso dei farmaci per il trattamento di supporto delle infezioni delle vie respiratorie in pediatria rappresenta una delle pratiche di più frequente ricorso. A fronte della grande popolarità di questi farmaci, le prove di efficacia a loro favore sono frequentemente estrapolate da studi effettuati sugli adulti, e i rari studi disponibili per l'età pediatrica non supportano l'efficacia della maggior parte delle molecole utilizzate per questo scopo. In alcuni casi, inoltre, alcuni principi attivi contenuti nei farmaci per il trattamento di supporto delle infezioni respiratorie sono associati ad effetti collaterali importanti.
Alla luce delle evidenze disponibili, nel bambino con infezione delle vie aeree superiori:
- i farmaci disponibili per il trattamento di supporto della malattia non sono in grado di abbreviarne il decorso;
- l'uso di farmaci antipiretici/antinfiammatori come il paracetamolo e l'ibuprofene è raccomandato per il trattamento sintomatico della febbre;
- l'uso dell'acido acetilsalicilico è controindicato sotto i 16 anni di età per il rischio di S. di Reye;
- l'uso dei decongestionanti nasali, sebbene associato a lieve miglioramento sintomatico per la vasocostrizione indotta, è controindicato nei bambini con età < 12 anni per i potenziali effetti collaterali anche gravi ad essi associati;
- l'uso di vapore per via inalatoria può conferire sollievo temporaneo ma non è raccomandato di routine;
- l'uso di steroidi per via inalatoria in assenza di asma o wheezing non è raccomandato;
- l'uso di sedativi della tosse non è raccomandato per l'assenza di prove di efficacia in pediatria. Questi farmaci possono inoltre esporre ad effetti collaterali anche gravi;
- l'uso di mucolitici o di espettoranti non è raccomandato per la mancanza di prove di efficacia di questi farmaci in pediatria;
- l'uso di antistaminici non è raccomandato per la mancanza di prove di efficacia in pediatria e per la documentazione di possibili gravi effetti collaterali;
- la terapia con farmaci omeopatici o fitoterapici, vitamina C o zinco, non è raccomandata per la mancanza di prove di efficacia.
Bibliografia
- Bielory L. Complementary and alternative interventions in asthma, allergy, and immunology. Ann Allergy Asthma Immunol 2004; 93 (2 Suppl 1): S45-54.
- Kligler B, Ulbricht C, Basch E, et al. Andrographis paniculata for the treatment of upper respiratory infection: a systematic review by the natural standard research collaboration. Explore (NY) 2006; 2: 25-9.
- Coon JT, Ernst E. Andrographis paniculata in the treatment of upper respiratory tract infections: a systematic review of safety and efficacy. Planta Med 2004; 70: 293-8.
- Poolsup N, Suthisisang C, Prathanturarug S, Asawamekin A, Chanchareon U. Andrographis paniculata in the symptomatic treatment of uncomplicated upper respiratory tract infection: systematic review of randomized controlled trials. J Clin Pharm Ther 2004; 29: 37-45.
- Càceres DD, Hancke JL, Burgos RA, Sandberg F, Wikman GK. Use of visual analogue scale measurements (VAS) to assess the effectiveness of standardized Andrographis paniculata extract SHA-10 in reducing the symptoms of common cold. A randomized double blind-placebo study. Phytomedicine 1999; 6: 217-23.
- Gabrielian ES, Shukarian AK, Goukasova GI, et al. A double blind, placebo-controlled study of Andrographis paniculata fixed combination Kan Jang in the treatment of acute upper respiratory tract infections including sinusitis. Phytomedicine 2002; 9: 589-97.
- Shakhova EG, Spasov AA, Ostrovski OV, Konovalova IV, Chernikov MV, Mel'nikova GI. Effectiveness of using the drug Kan-Yang in children with acute respiratory viral infection (clinico-functional data). Vestn Otorinolaringol 2003; 3: 48-50.
- Hofmann D, Hecker M., Völp A. Efficacy of dry extract of ivy leaves in children with bronchial asthma - a review of randomized controlled trials. Phytomedicine Vol. 10 (2-3); 213: 20, 2003.
- Caruso TJ, Gwaltney JM Jr. Treatment of the common cold with echinacea: a structured review. Clin Infect Dis 2005; 40: 807-10. Epub 2005 Feb 18.
- Linde K, Barrett B, Wölkart K, Bauer R, Melchart D. Echinacea for preventing and treating the common cold. Cochrane Database Syst Rev 2006; 1: CD000530.
- Cohen HA, Varsano I, Kahan E, Sarrell EM, Uziel Y. Effectiveness of an herbal preparation containing echinacea, propolis, and vitamin C in preventing respiratory tract infections in children: a randomized, double-blind, placebo-controlled, multicenter study. Arch Pediatr Adolesc Med 2004; 158: 217-21.
- Taylor JA, Weber W, Standish L, et al. Efficacy and safety of echinacea in treating upper respiratory tract infections in children: a randomized controlled trial. JAMA 2003; 290: 2824-30.
- Treatment of the common cold. Am Fam Physician 2007; 75: 515-20.
- Koenig K, Roehr CC. Does treatment with Echinacea purpurea effectively shorten the course of upper respiratory tract infections in children? Arch Dis Child 2006; 91: 535-7.
- Conrad A, Kolodziej H, Schulz V. Pelargonium sidoidesextract (EPs 7630): registration confirms efficacy and safety. Wien Med Wochenschr 2007; 157: 331-6.
- Agbabiaka TB, Guo R, Ernst E. Pelargonium sidoides for acute bronchitis: a systematic review and meta-analysis. Phytomedicine 2008; Epub ahead of print.
- Haidvogl M, Heger M. Treatment effect and safety of EPs7630-solution in acute bronchitis in childhood: Report of a multicentre observational study. Phytomedicine 2007; 14 S1: 60-64.
- Matthys H, Kamin W, Funk P, Heger M. Pelargonium sidoides preparation (EPs 7630) in the treatment of acute bronchitis in adults and children. Phytomedicine 2007;14 S6:69-73.
- Bereznoy VV, Riley DS, Wassmer G, Heger M. Efficacy of extract of Pelargonium sidoides in children with acute non-group A beta-hemolytic streptococcus tonsillopharyngitis: a randomized, double-blind, placebo-controlled trial. Altern Ther Health Med 2003; 9: 68-79.
- Aggarwal R, Sentz J, Miller MA. Role of zinc administration in prevention of childhood diarrhea and respiratory illnesses: a meta-analysis. Pediatrics 2007; 119: 1120-30.
- Eby GA, Davis DR, Halcomb WW. Reduction in duration of common colds by zinc gluconate lozenges in a double-blind study. Antimicrob Agents Chemother 1984; 25: 20-4.
- Kurugöl Z, Akilli M, Bayram N, Koturoglu G. The prophylactic and therapeutic effectiveness of zinc sulphate on common cold in children. Acta Paediatr 2006; 95: 1175-81.
- Macknin ML, Piedmonte M, Calendine C, Janosky J, Wald E. Zinc gluconate lozenges for treating the common cold in children: a randomized controlled trial. JAMA 1998; 279: 1962-7.
- Eby GA, Halcomb WW. Ineffectiveness of zinc gluconate nasal spray and zinc orotate lozenges in common-cold treatment: a double-blind, placebo-controlled clinical trial. Altern Ther Health Med 2006; 12: 34-8.
- Turner RB, Cetnarowski WE. Effect of treatment with zinc gluconate or zinc acetate on experimental and natural colds. Clin Infect Dis 2000; 31: 1202-8.
- Arroll B. Non-antibiotic treatments for upper-respiratory tract infections (common cold). Respir Med 2005; 99: 1477-84.
- Carr RR, Nahata MC. Complementary and alternative medicine for upper-respiratory-tract infection in children. Am J Health Syst Pharm 2006; 63: 33-9.
Risorse
Ancora ... Antibiotici
Riferimenti
I punti chiave
- Le infezioni delle vie respiratorie superiori sono condizioni cliniche che si risolvono spontaneamente entro pochi giorni, causate in massima parte da virus.
- L'uso di farmaci antipiretici o antinfiammatori per il trattamento della febbre e della sintomatologia generale è appropriato in queste forme.
- L'efficacia di decongestionanti nasali in età pediatrica rimane non provata e questi farmaci possono provocare effetti collaterali anche gravi.
- L'uso di farmaci per via inalatoria non è supportato da prove di efficacia nel bambino.
- L'uso di sedativi della tosse, seppure ampiamente utilizzati, non è supportato da studi clinici in pediatria. Gli studi disponibili non dimostrano vantaggi di questi farmaci rispetto al placebo e possono esporre ad effetti collaterali anche gravi.
- L'uso dei mucolitici e degli espettoranti non trova giustificazione nei rari studi disponibili, che non forniscono prove di efficacia in pediatria.
- L'uso degli antistaminici non è supportato da prove di efficacia e può essere associato ad effetti collaterali.
- L'uso della omeopatia, della fitoterapia e della vitamina C non è supportato da studi clinici adeguati di efficacia e sicurezza in pediatria.
Bibliografia
- American Academy of Pediatrics. Use of codeine and dextromethorphan containing cough remedies in children. Pediatrics 1997; 99: 918-20.
- Taylor JA, Novack AH, Almquist JR, Rogers JE. Efficacy of cough suppressants in children. J Pediatr 1993; 122: 799-802.
- Paul IM, Yoder KE, Crowell KR, et al. Effect of dextrometorphan, diphenhydramine, and placebo on nocturnal cough and sleep quality for coughing children and their parents. Pediatrics 2004; 114: e85-e90.
- Paul IM, Beiler J, McMonagle A, Shaffer ML, Duda L, Berlin CM. Effect of honey, dextromethorphan, and no treatment on nocturnal cough and sleep quality for coughing children and their parents. Arch Pediatr Adolesc Med 2007; 161: 1140-6.
- Yoder KE, Shaffer ML, La Tournous SJ, Paul IM. Child assessment of dextromethorphan, diphenhydramine, and placebo for nocturnal cough due to upper respiratory infection. Clin Pediatr (Phila) 2006; 45: 633.
- Aliprandi P, Castelli C, Bernorio S, Dell'Abate E, Carrara M. Levocloperastine in the treatment of chronic nonproductive cough: comparative efficacy versus standard antitussive agents. Drugs Exp Clin Res 2004; 30: 133-41.
- Banderali G, Riva E, Fiocchi A, Cordaro CI, Giovannini M. Efficacy and tolerability of levodropropizine and dropropizine in children with non-productive cough. J Int Med Res 1995; 23: 175-83.
- Perrott DA, Piira T, Goodenough B, Champion GD. Efficacy and safety of acetaminophen vs ibuprofen for treating children's pain or fever: a metaanalysis. Arch Ped Adol Med 2004; 158: 521-6.
- >Goldman RD. Efficacy and safety of acetaminophen versus ibuprofen for treating children's pain or fever: a meta-analysis. J Ped 2005; 146: 142-3.
- Schachtel BP, Thoden WR. A placebo-controlled model for assaying systemic analgesics in children. Clin Phar Ther 1993; 53: 593-601.
- Lesko SM, Mitchell AA. An assessment of the safety of pediatric ibuprofen. A practitioner-based randomized clinical trial. JAMA 1995; 273: 929-33.
- Ulukol B, Koksal Y, Cin S. Assessment of the efficacy and safety of paracetamol, ibuprofen and nimesulide in children with upper respiratory tract infections. Eur J Clin Phar 1999; 55: 615-8.
- Hersh E, Moore P, Ross G. Over-the-counter analgesics and antipyretics: a critical assessment. Clin Ther 2000; 22: 500-48.
- Doyle G, Furey S, Berlin R, et al. Gastrointestinal safety and tolerance of ibuprofen at maximum over-the-counter dose. Alim Phar Ther 1999; 13: 897-906.
- Kellstein DE, Waksman JA, Furey SA, Binstok G, Cooper SA. The safety profile of non-prescription ibuprofen in multiple-dose use: a meta-analysis. J Clin Pharm 1999; 39: 520-32.
- Colgan MT, Mintz AA. The comparative antipyretic effect of N-acetyl-p-aminophenol and acetylsalicylic acid. J Ped 1957; 50: 552-5.
- Yaffe SJ. Comparative efficacy of aspirin and acetaminophen in the reduction of fever in children. Arch Int Med 1981; 141: 286-92.
- Heubi JE, Partin JC, Partin JS, Schubert WK. Reye's syndrome: current concepts. Hepatology 1987; 7: 155-64.
- Pinsky P, Hurwitz ES, Schonberger LB, Gunn WJ. Reye's syndrome and aspirin. Evidence for a dose-response relationship. J Am Med Ass 1988; 260: 657-61.
- Taverner D, Latte J. Nasal decongestants for the common cold. Cochrane Database Syst Rev 2007; 24.
- Clemens CJ, Taylor JA, Almquist JR, Quinn HC, Mehta A, Naylor GS. Is an antihistamine-decongestant combination effective in temporarily relieving symptoms of the common cold in preschool children? J Pediatr 1997; 130: 463-6.
- Hutton N, Wilson MH, Mellits ED, et al. Effectiveness of an antihistamine-decongestant combination for young children with the common cold: a randomized, controlled clinical trial. J Pediatr 1991; 118: 125-30.
- Bucaretchi F, Dragosavac S, Vieira RJ. Acute exposure to imidazoline derivatives in children. Jornal de Pediatria (RioJ) 2003; 79: 519-24.
- Mahieu LM, Rooman RP, Goossens E. Imidazoline intoxication in children. Eur J Pediatr 1993; 152: 944-6.
- Vitezic D, Rozmanic V, Franulovic J, Ahel V, Matesic D. Naphazoline nasal drops intoxication in children. Arh Hig Rada Toksikol 1994; 45: 25-9.
- van Cauwenberge P, Bachert C, Passalacqua G, et al. Consensus statement on the treatment of allergic rhinitis. European Academy of Allergology and Clinical Immunology. Allergy 2000; 55: 116-34.
- Agenzia Italiana del Farmaco. Decongestionanti nasali nei bambini: i rischi superano i benefici. Bollettino d'Informazione sui Farmaci 2007 - estratto anticipato; 2: 1-8. www.agenziafarmaco.it
- Ophir D, Elad Y. Effects of steam inhalation on nasal patency and nasal symptoms in patients with the common cold. Am J Otolaryngol 1987; 8: 149-53.
- Tyrrell D, Barrow I, Arthur J. Local hyperthermia benefits natural and experimental common colds. BMJ 1989; 298: 1280-3.
- Forstall GJ, Macknin ML, Yen-Lieberman BR, Medendrop SV. Effect of inhaling heated vapor on symptoms of the common cold. JAMA 1994; 271: 1109-11.
- Knight V, Gilbert BE. Aerosol treatment of respiratory viral disease. Lung 1990; 168 (Suppl): 406-13.
- LiPuma JJ. Microbiological and immunologic considerations with aerosolized drug delivery. Chest 2001; 120 (3 Suppl): 118S-123S.
- Hay AD, Wilson AD. The natural history of acute cough in children aged 0 to 4 years in primary care: a systematic review. Br J Gen Pract 2002; 52: 401-9.
- American Academy of Pediatrics. Use of codeine and dextromethorphan containing cough remedies in children. Pediatrics 1997; 99: 918-20.
- Schroeder K, Fahey T. Should we advise parents to administer over the counter cough medicines for acute cough? Systematic review of randomised controlled trials. Arch Dis Child 2002; 86: 170-5.
- Schroeder K, Fahey T. Over the counter medications for acute cough in children and adults in ambulatory settings. Cochrane Database Syst Rev 2004; 4: CD001831.
- Smucny J, Becker l, Glazier R. Beta2-agonist for acute bronchitis. Cochrane Database of Systematic Reviews 2006;4: CD001726.
- Taylor JA, Novack AH, Almquist JR, Rogers JE. Efficacy of cough suppressants in children. J Pediatr 1993; 122: 799- 802.
- Paul IM, Yoder KE, Crowell KR, et al. Effect of dextrometorphan, diphenhydramine, and placebo on nocturnal cough and sleep quality for coughing children and their parents. Pediatrics 2004; 114: e85-e90.
- Paul IM, Beiler J, McMonagle A, Shaffer ML, Duda L, Berlin CM. Effect of honey, dextromethorphan, and no treatment on nocturnal cough and sleep quality for coughing children and their parents. Arch Pediatr Adolesc Med 2007; 161: 1140-6.
- Aliprandi P, Castelli C, Bernorio S, Dell'Abate E, Carrara M. Levocloperastine in the treatment of chronic nonproductive cough: comparative efficacy versus standard antitussive agents. Drugs Exp Clin Res 2004; 30: 133-41.
- Banderali G, Riva E, Fiocchi A, Cordaro CI, Giovannini M. Efficacy and tolerability of levodropropizine and dropropizine in children with non-productive cough. J Int Med Res 1995; 23: 175-83.
- Nespoli L, Monafo V, Bonetti F, et al. Valutazione clinica dell'attività della letosteina nel trattamento della bronchite acuta febbrile in età pediatrica. Indagine controllata in doppio cieco vs placebo. Minerva Pediatr 1989; 41: 515-20.
- Chang CC, Cheng AC, Chang AB. Over-the-counter (OTC) medications to reduce cough as an adjunct to antibiotics for acute pneumonia in children and adults. Cochrane Database Syst Rev 2007; CD006088.
- Menniti-Ippolito F, Traversa G, Da Cas R, Capriano A, Bolli M. Sicurezza dei farmaci in pediatria. Rapporti Istisan 2006; 06/16.
- Nacleiro RM, Proud D, Kagey-Sobotka A, Lichtenstein LM, Hendley JO, Gwaltney JR. Is histamine responsible for the symptoms of rhinovirus colds? A look at the inflammatory mediators following infection. Pediatr Infec Dis J 1988; 7: 215-42.
- Welliver RC. The role of antihistamines in upper respiratory tract infections. J All Clin Immunol 1990; 86: 633-7.
- De Sutter AIM, Lemiengre M, Campbell H. Antihistamines for the common cold. Cochrane Database Syst Rev 2003, Issue 3. Art. No.: CD001267.
- Hugenin M, Martin Du Pan R, Oppikofer-Doody AM. Astemizole in the treatment of acute rhinopharyngitis (common cold). Double blind study in pediatrics [L'Astémizole dans le traitement de la rhinopharyngite aiguë (common cold). Etude en double aveugle en pédiatrie]. Rev Med Suisse Romande 1988; 108: 961-6.
- Hutton N, Hoover Wilson M, Mellits ED, Baumgarter R, Wissow LS, Bonucelli C. Effectiveness of an antihistamine-decongestant combination for young children with the common cold: a randomized, controlled clinical trial. J Pediatrics 1991; 118: 123-30.
- Litovitz TL, Klein-Schwartz W, White S, Cobaugh DJ, Youniss J, Omslaer JC, Drab A, Benson BE. 2000 Annual report of the American Association of Poison Control Centers. Toxic Exposure Surveillance System.
- Sharfstein, JM, North M, Serwint JR. Over the Counter but no longer under the radar-pediatric cough and cold medications. N Engl J Med 2007; 357: 23.
- Wingert W E, Mundy L A, Collins G L, Chmara ES. Possible role of pseudoephedrine and other over-the-counter cold medications in the deaths of very young children. J Forensic Sci 2007; 52: 487-90.
- Zollman C, Vickers A. ABC of complementary medicine: what is complementary medicine? BMJ 1999; 319.
- Schmidt K, Pittler M, Ernst E. Bias in alternative medicines still rife but is diminishing. BMJ 2001; 323: 1071.
- Kleijnen J, Knipschild P, Riet G. Clinical trials of homoeopathy. BMJ 1991; 302: 316-23.
- Boissel JP, Cucherat M, Haugh M, Gauthier E. Critical literature review on the effectiveness of homoeopathy: overview of data from homoeopathic medicine trials. Brussels, Belgium: Homoeopathic Medicine Research Group. Report to the European Commission 1996: 195-210.
- Linde K, Melchart D. Randomized controlled trials of individualized homeopathy: a state-of-the-art review. J Alter Complement Med 1998; 4: 371-88.
- Cucherat M, Haugh MC, Gooch M, Boissel JP. Evidence of clinical efficacy of homeopathy: a meta-analysis of clinical trials. Eur J Clin Pharmacol 2000; 56: 27-33.
- Shang A, Huwiler-Müntener K, Nartey L, et al. Are the clinical effects of homoeopathy placebo effects? Comparative study of placebo-controlled trials of homoeopathy and allopathy. Lancet 2005; 366: 726-32.
- Ernst E. A systematic review of systematic reviews of homeopathy. Br J Clin Pharmacol 2002; Vol. 54 No. 6: 577.
- Altunç U, Pittler MH, Ernst E. Homeopathy for childhood and adolescence aliments: systematic review of randomized clinical trials. Mayo Clin Proc 2007; 82: 69-75.
- Haidvogl M, Riley DS, Heger M, et al. Homeopathic and conventional treatment for acute respiratory and ear complaints: a comparative study on outcome in the primary care setting. BMC Complement Altern Med 2007; 7: 7.
- Friese KH, Zabalotnyi DI. Homeopathy in acute rhinosinusitis: a double-blind, placebo controlled study shows the efficiency and tolerability of a homeopathic combination remedy. HNO 2007; 55: 271-7.
- Trichard M, Chaufferin G, Nicoloyannis N. Pharmacoeconomic comparison between homeopathic and antibiotic treatment strategies in recurrent acute rhinopharyngitis in children. Homeopathy 2005; 94: 3-9.
- MacKay D. Can CAM therapies help reduce antibiotic resistance? Altern Med Rev 2003; 8: 28-42.
- Gardiner P, Riley DS. Herbs to homeopathy-medicinal products for children. Pediatr Clin North Am 2007; 54: 859-74.
- Dobrilla G, Coluzzi G. Fitoterapia. Roma: Il Pensiero Scientifico Editore, 2005.
- Murgia V, Ventriglia G. Fitoterapia in pediatria. Milano: Masson, 2006.
- Pittler MH, Ernst E. Clinical effectiveness of garlic (Allium sativum). Mol Nutr Food Res 2007; 51: 382-5.
- Josling P. Preventing the common cold with a garlic supplement: a double-blind, placebo-controlled survey. Adv Ther 2001;18: 189-93.